1 Introduction
2 Pourquoi une action sur le critère intermédiaire peut ne pas apporter de bénéfice clinique
3 Méthode de validation des surrogates
4 Limites des études de validation de surrogate [new]
5 Extrapolabilité/transposabilité
Avant d’être utilisé en pratique, un nouveau traitement doit apporter la preuve qu’il améliore le devenir des patients sur des critères cliniquement pertinents (démonstration d’un bénéfice cliniquement pertinent).
Par rapport à la simple mise en évidence d’un effet pharmacologique sur un critère intermédiaire, cette démonstration demande un plus grand nombre de patients ou une durée de suivi des patients plus importante.
Par exemple, la mise en évidence de l’effet d’un traitement contre l’ostéoporose sur la prévention des fractures du col du fémur chez la personne âgée nécessite un suivi de plusieurs années, le but du traitement étant de ralentir la perte de densité osseuse survenant au fil des années après la ménopause pour retarder le moment où le seuil fracturaire est atteint
D’où l’idée de chercher si certains critères intermédiaires ne pourraient pas être des surrogates (critères de substitution), c’est-à-dire des critères pour lesquels l’observation d’un effet d’un traitement à leur niveau impliquerait forcément un effet sur le critère clinique approprié. Dans ce cas, la simple mise en évidence d’un effet pharmacologique sur ce type de critère équivaudrait à la démonstration du bénéfice clinique,sans devoir le démontre directement dans l’essai sur le critère clinique.
Avec l’exemple précédent, cela revient à s’interroger si la mise en évidence d’un effet sur la densité osseuse ne suffirait pas à conclure que le nouveau traitement réduit la fréquence des fractures. Si c’est le cas, un essai portant la densité osseuse demandera nettement moins de sujets et de suivi qu’un essai sur les fractures, mais montrerait la valeur du traitement pour la prévention des fractures (sans avoir besoin de le démontrer par lui-même).
Cependant, tous les critères intermédiaires ne sont pas des surrogates, et il est nécessaire de le démontrer spécifique, au cas par cas et par une approche rigoureuse qu’un critère intermédiaire à bien les propriétés nécessaires pour être un surrogate.
Critères cliniques. Les critères cliniques sont des critères de jugement qui correspondent directement avec la problématique clinique que pose la maladie. La mise en évidence d’un effet du traitement à leur niveau assure que celui-ci apporte bien le bénéfice clinique recherché. Par exemple dans l’hypertension artérielle, les critères cliniques sont les évènements cardiovasculaires(infarctus du myocarde ou AVC) mortels et non mortels ou les décès de cause cardiovasculaire ; pour les cancers au stade avancé ou métastatique, le décès ; pour l’ostéoporose les fractures vertébrales ou des os longs ; etc.
Critères intermédiaires . Les critères intermédiaires sont de la catégorie des signes des maladies ou de leur mécanisme d’action. Ils ne mesurent pas directement les conséquences de la maladie. Ils servent à montre une activité biologique des traitements (activité anticancer, action pharmacologique). La mise en évidence de l’effet d’un traitement à leur niveau est insuffisante, car rien ne garantit que cet effet se traduit par un bénéfice clinique. C’est par exemple la pression artérielle systolique dans l’hypertension artérielle, la réponse tumorale avec un traitement du cancer ou la densité osseuse dans l’ostéoporose.
Pour être critère de substitution (surrogate ) et, ainsi, être utilisé dans un essai randomisé à la place d’un critère clinique, un critère intermédiaire doit garantir que l’observation d’un effet d’un traitement à son niveau prédit avec certitude un effet de ce traitement au niveau du critère clinique [1].
D’emblée il faut insister qu’il s’agît ici de la prédiction d’un effet traitement (objectivé par un hazard ratio, ou une différence de moyenne par exemple) par un autre effet traitement (objectivé lui aussi par un hazard ou une différence de moyenne par exemple) et non pas, de la prédiction indivduelle de la probabilité de survenue d’un évènement clinique par un facteur pronostique ou un facteur de risque (cf. section Erreur ! Source du renvoi introuvable. )
La FDA définit les surrogates de la manière suivante note n° 1 :
« a surrogate endpoint is a marker, such as a laboratory measurement, radiographic image, physical sign, or other measure that is thought to predict clinical benefit, but is not itself a measure of clinical benefit”
Le critère de substitution est une problématique d’évaluation des traitements : trouver un substitut aux critères cliniques afin de permettre la réalisation d’essais randomisés plus courts et nécessitant peu de patients. Il ne s’agit donc pas d’une problématique médicale, comme comprendre par quel mécanisme passe le bénéfice clinique apporté par un traitement. Cette recherche d’explication est le domaine de la « mediation analysis » [3].
Deux guidelines de rédaction SPIRIT et CONSORT précisent les informations indispensables à mentionner dans les protocoles (SPIRIT-surrogate [2]) et les publications (CONSORT-surrogate [3]) des essais cliniques ayant comme critère de jugement principal un surrogate.
On peut faire le constat que dans la littérature, les termes de proxy, critère intermédiaire et de surrogate sont souvent interchangeables, ce qui témoignent de la confusion dans les concepts. La Food and Drug Administration a produit une liste de critères intermédiaires acceptés pour l’'enregistrement des médicaments en utilisant le terme surrogate (https://www.fda.gov/drugs/development-resources/surrogate-endpoint-resources-drug-and-biologic-development). Une analyse de la pertinence de ces critères a montré que ces critères ne relevaient pas de la surrogacy dans les champs médicaux non-oncologiques [4]. L’association entre critère intermédiaire et critère clinique ne fait pas un surrogate
L’existence d’une association entre un critère intermédiaire (biomarqueurs) et un critère clinique (décès, évènement) n’est pas suffisante pour faire de ce critère intermédiaire un surrogate. Cette association (qui peut être observée au niveau épidémiologique par exemple) ne garantit pas qu’une modification provoquée du critère intermédiaire par le traitement se traduira automatiquement par un bénéfice proportionné au niveau du critère clinique. Cette association démontre seulement la valeur pronostique du critère intermédiaire. Dans le jargon des méthodes de validation des surrogates elle est dénommée « subject level correlation » .
En effet, par définition, une association de ce type montre qu’il existe une relation statistique à travers les patients entre les valeurs du critère intermédiaire (par exemple la pression artérielle systolique) et celles du critère clinique (par exemple la probabilité de faire un AVC à 5 ans). Plus un sujet a une valeur élevée (ou l’inverse) au niveau du critère intermédiaire, plus il est probable, en moyenne, qu’il aura une valeur élevée sur le critère clinique (d’où l’appellation de subject level correlation ).
La définition du surrogate se réfère quant à elle à une association entre les effets traitements et non pas entre les critères. Comme les effets traitements ne peuvent être mesurés qu’à l’aide d’un essai, cette association sera dénommée « trial level correlation » (cf. section Erreur ! Source du renvoi introuvable. ).
En effet, de très nombreux exemples montrent qu’une association entre le critère intermédiaire et le critère clinique n’est pas suffisante pour garantir que tout traitement agissant sur le critère intermédiaire provoquera un bénéfice sur le critère clinique.
Epidémiologiquement, il existe une forte relation au niveau de sujets, entre le niveau de cholestérolémie et le risque cardiovasculaire [5][6]. Cette relation a été très bien identifiée dans les études épidémiologiques historiques comme MRFIT ou l’étude de Framingham :
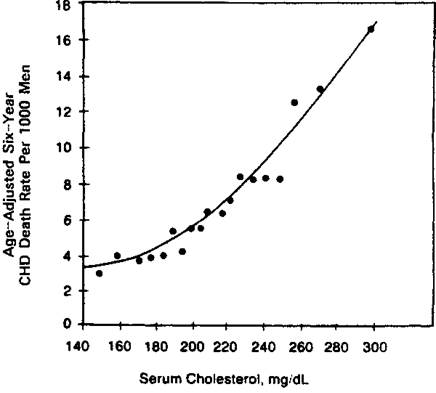
Association statistique entre la cholestérolémie et le risque de décès coronariens identifiée dans l’étude épidémiologique MRFIT [7].
Cependant plusieurs molécules hypocholestérolémiantes n’ont pas montré de bénéfice clinique sur les événements coronariens comme l’acide nicotinique dans l’essai de grande taille HPS2-THRIVE [8] :
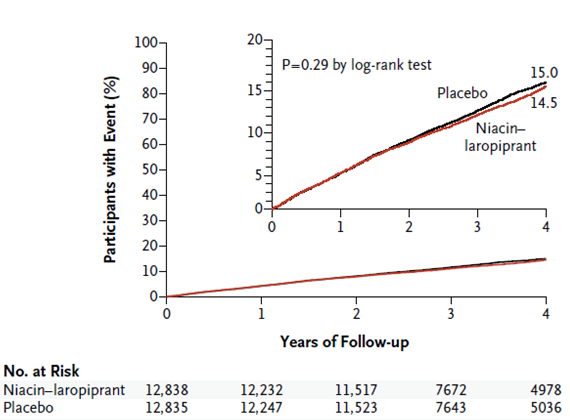
Et cela malgré un effet pharmacologique sur les différents paramètres lipidiques :
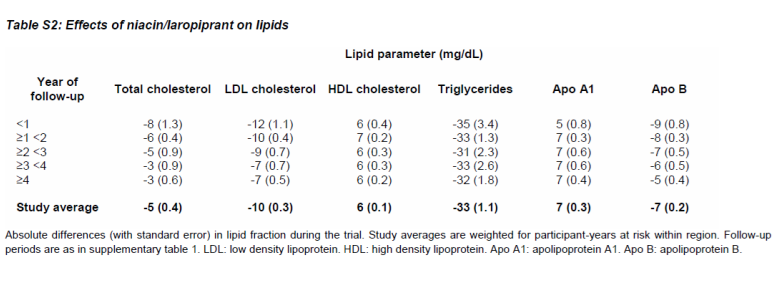
Un autre essai similaire de grande taille de la niacine, AIM-HIGH [7], donne le même résultat.
Le fluorure de sodium stimule la formation osseuse et accroit la densité osseuse. En raison de ces effets, il a été envisagé comme traitement préventif de l’ostéoporose de la femme ménopausée. Dans un essai randomisé [9] contre placebo réalisé chez 202 femmes ménopausées et suivies pendant 4 ans, le fluorure de sodium augmente la densité osseuse de la colonne lombaire de façon hautement significative (p<0,001). Cependant, des nouvelles fractures vertébrales surviennent plus fréquemment sous fluorure de sodium que sous placebo (163 comparé à 136) ainsi que des fractures non vertébrales (72 versus 24, p=0,01). Cet essai conclut que la forme de fluorure utilisé augmente certains aspects de la densité osseuse, mais rend les os plus fragiles. L’utilisation de la densité osseuse comme critère de substitution n’aurait pas permis de mettre en évidence ces effets délétères qui enlèvent pourtant tout intérêt au traitement.
La simple existence de ces contre-exemples montre qu’une association au niveau des sujets entre les critères intermédiaire et clinique (subject level correlation) n’implique pas que le critère intermédiaire soit un surrogate et qu’il soit possible d’inférer un bénéfice clinique à partir d’un effet sur le critère intermédiaire. Le Tableau 1 liste une série d’exemples où des essais ont réfuté la valeur de surrogacy de simple association entre critères au niveau sujet pourtant bien établies, en ne montrant pas de bénéfice clinique de molécule impactant pourtant favorablement le critère intermédiaire.
Tableau 1 - Exemples de réfutation de la valeur de surrogacy d’une association entre critères au niveau sujet pourtant bien établie par des molécules ayant bien une action sur le biomarqueur, mais qui ont échouées à mettre en évidence un bénéfice clinique.
Biomarqueurs ayant un lien avec les critères cliniques et susceptibles d’être des surrogates potentiels |
Essai qui ont échoué à mettre en évidence un bénéfice clinique avec une molécule ayant une action sur le biomarqueur |
HbA1 et événements cardiovasculaires (macrovasculaires) |
Essai d’intensification PREVENT *** ins *** |
Vitamine D et événements cardiovasculaires |
Méta-analyse de 21 essais randomisés [10] |
Vitamine D et événements osseux en l’absence de carence |
Essai VITAL [11] |
LDL et événements cardiovasculaires |
HPS2-THRIVE [8] et AIM-HIGH [7] avec la niacine |
HDL et événements cardiovasculaires |
ILLUMINATE [6] avec le torcétrapib |
Triglycérides et événements cardiovasculaires |
FIELD avec le fénofibrate [12]. PROMINENT avec le pemafibrate [13] |
PFS dans les cancers du sein avec mutation BRCA |
ARIEL 4 avec le rucaparib en 3ème ligne suggérant une augmentation de la mortalité conduisant au retrait de l’AMM note n° 2 pour cette indication, AMM donnée sur la base des résultats de PFS [14]. |
Il existe des contre-exemples même pour des facteurs qui peuvent raisonnablement être considérés comme causaux (en raison de la force de l’association, de l’existence d’une relation dose effet et d’une plausibilité biologique forte ou en raison d’une démonstration de casualité apportée par une étude de randomisation mendélienne robuste). Sur ce point, il est souvent assez difficile, cognitivement, d’accepter qu’une relation causale n’est pas suffisant pour établir un surrogate. La suppression d’une cause entraine forcément la disparition des conséquences de la cause. Certes, mais l’action qui supprime la cause (ou plus vraisemblablement la réduit) peut avoir d’autres actions qui s’avèrent délétères et impacte négativement le critère clinique : effets indésirables graves (cf. section 2.2), effets off-target (cf. section 2.1) ou mécanisme plus complexe qu’une cause unique et directe (cf. section 2.3). De ce fait, même en supprimant une cause d’un événement clinique, rien ne garantit, avant que cela ne soit parfaitement démontré, que cette action aura un bilan positif sur le critère clinique et apportera, au total, un bénéfice clinique.
Ainsi, tout facteur pronostique ou tout facteur de risque n’est pas, de-facto, un surrogate pour l’évaluation des traitements. Les surrogates doivent vérifier des propriétés qui leur sont propres et qui vont au-delà de la simple association statistique critère intermédiaire – critère clinique.
Parfois, un effet pharmacologique est considéré comme étant un surrogate à partir du moment où il existe un essai clinique qui a montré un bénéfice sur le critère clinique avec une molécule produisant cet effet pharmacologique [15]. Par exemple, comme les essais des statines montrent une réduction de la morbi-mortalité cardiovasculaire et que les statines entrainent une baisse du LDL cholestérol, le LDL est un surrogate des événements cardiovasculaires. Ce raisonnement ne peut pas être retenu par manque de représentativité (est-ce que toutes les molécules de différentes classes produisant cet effet pharmacologie ont conduit à un bénéfice sur le critère clinique ?) et en raison de nombreux facteurs de confusion possible (bénéfice apporté par un autre mécanisme que l’effet pharmacologique considéré). De nombreux contre-exemples existent de molécules ayant échoué à montrer un bénéfice clinique alors qu’elles produisent le même effet pharmacologique que d'autres molécules ayant, quant à elles, parfaitement démontré un bénéfice clinique (comme les exemples de la niacine, du fluorure de sodium développé précédemment).
[1] FDA Guidance for Industry Expedited Programs for Serious Conditions––Drugs and Biologics
[2] https://www.ema.europa.eu/en/news/ema-recommends-restricting-use-cancer-medicine-rubraca