2 Pourquoi une action sur le critère intermédiaire peut ne pas apporter de bénéfice clinique
3 Méthode de validation des surrogates
4 Limites des études de validation de surrogate [new]
4.1 Limites liées à la nature rétrospective des études, HARKing, p hacking
5 Extrapolabilité/transposabilité
La démonstration d’une très forte corrélation des effets n’est pas suffisante pour faire accepter un surrogate. Ces travaux d’évaluation de la surrogacy sont, par définition, rétrospectifs, et sont donc exposés à plusieurs problématiques dans la méthodologie de leur réalisation et peuvent avoir de nombreuses limites.
Les études de validation des surrogates sont avant tout des revues systématiques et des méta-analyses. Elles héritent des problématiques de ces techniques liées au caractère rétrospectif du travail induisant la possibilité de p hacking [32, 33] et de HARKing [34].
Les résultats de l’analyse de corrélation dépendent directement des études retenues pour effectuer cette recherche. Il est facile, du fait du caractère rétrospectif, de tester toutes les combinaisons possibles d’études et d’écrire ensuite le protocole et les critères de sélection des études. Compte tenu de la complexité de la littérature, de la multiplicité des études, ces manipulations de données sont difficiles à détecter. La fréquence de ces pratiques fait que l’on estime que seuls 20% des revues systématiques et méta-analyses publiées (quel que soit leur objectif, pas seulement celles destinées à évaluer un candidat surrogate) sont correctes méthodologiquement [35][36].
Il existe aussi une explosion combinatoire dans la façon dont peuvent être conduites les analyses de surrogacy en raison de la multiplicité des choix d’analyse possibles :
Ainsi, du fait de la nature rétrospective, rien n’empêche que de très nombreuses analyses soient réalisées avant d’obtenir l’analyse qui produit les résultats escomptés et qui sera finalement la seule présentée comme validation du surrogate.
En se basant sur ce qui a été observé de manière générale pour toutes les études rétrospectives (et en particulier les méta-analyses), il est raisonnable de conjecturer qu’il est possible d’obtenir dans ces travaux tous les résultats possibles en faveur ou en défaveur de la surrogacy. Ce point est d’ores et déjà illustré lorsque plusieurs travaux cherchant à établir la même surrogacy sont disponibles et donnent des résultats et des conclusions différents comme c’est le cas par exemple avec le cholestérol ou ses sous-fractions. [37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49].
Pour limiter un peu la flexibilité des analyses, des
guidelines statistiques [50, 51] ont été élaborés et pré-spécifient un certain nombre de principes d’analyse
comme l’utilisation d’effet traitement relatif, l’utilisation de l’odds ratio
avec les critères binaires (pour ses propriétés de symétrie et de domaine de
définition), avec une transformation logarithmique pour retrouver les
hypothèses de la régression (variables variant de *** m:r *** 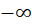 à *** m:r ***
à *** m:r *** 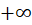 , hétéroscédasticité).
De même, le modèle linéaire s’impose en l’absence de justification biologique
forte pour une autre forme de modèle, en raison du principe de parcimonie du
rasoir d’Ockham.
, hétéroscédasticité).
De même, le modèle linéaire s’impose en l’absence de justification biologique
forte pour une autre forme de modèle, en raison du principe de parcimonie du
rasoir d’Ockham.
Pour éviter ces travers et assurer une certaine crédibilité aux résultats produits, ces travaux doivent être réalisés suivant un protocole et un plan d’analyse statistique fixant a priori les choix possibles décrits ci-dessus et établis avant toute analyse exploratoire des données, enregistrés et accompagnés dans le rapport ou la publication d’une attestation que les résultats présentés sont conformes à l’analyse préétablie (ou une description des changements avec leur justification).
En particulier la recherche des essais participants à la recherche de la corrélation des effets doit être impérativement réalisée par une réelle revue systématique afin d’éviter toute sélection arbitraire des essais afin d’obtenir le résultat souhaité. La méthode de cette revue systématique doit être fixée au protocole et conforme à l’état de l’art (Cochrane Handbook par exemple). En particulier les critères de sélection des essais doivent être clairement énoncés à priori et justifiés. Une description des essais exclus avec la raison d’exclusion permettra de vérifier la rigueur de l’application de ces critères.
L’UE, dans le cadre du Join Clinical Assessment (JCA), a préciser ses attentes note n° 4 sur la validation des surrogates [52].
[4] HTA CG. Guidance on outcomes for joint clinical assessments. Localisation https://health.ec.europa.eu/publications/guidance-outcomes-joint-clinical-assessments_en