2 Problématiques engendrées par les crossovers
3 Prise en compte des crossovers dans l’analyse de la survie
3.1 Analyse en intention de traiter (estimand « treatment policy »)
3.2 Analyse en traitement reçu
3.4 Méthodes de correction
Différentes méthodes ont été proposées pour corriger le résultat de survie d’un essai de l’effet des crossovers.
Le principe général de ces méthodes est de modifier la survie observée des patients du groupe contrôle ayant fait un crossover à l’aide d’une estimation de l’effet du nouveau traitement sur la mortalité, afin de calculer ce qu’aurait été la mortalité du groupe contrôle en l’absence de crossover. Une fois la mortalité du groupe contrôle corrigée, elle est comparée à celle observée dans le groupe traité pour déterminer l’effet du nouveau traitement sur la mortalité.
Les limites de ces approches résident dans les hypothèses sous-jacentes et dans le fait qu’il est nécessaire d’introduire une estimation de l’effet sur la survie globale (OS) pour obtenir l’effet sur l’OS !
Le principe général de ces méthodes peut être expliqué de façon simpliste de la manière suivante. Imaginons que le traitement augmente la durée de survie note n° 3 en la multipliant par un facteur Ψ (Ψ>1). Pour les patients du groupe contrôle ayant fait un crossover à la progression, leur temps de survie est donc multiplié par le nouveau traitement par Ψ par rapport à ce qu’il aurait dû être. Il est donc possible de retrouver cette durée de survie, sans crossover, en divisant par Ψ. Pour les autres patients du groupe contrôle, la survie réellement observée est utilisée.
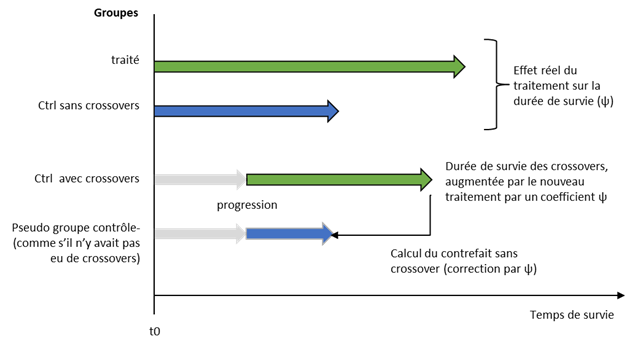
Les flèches de couleur (vert pour le groupe expérimental et bleu pour le groupe contrôle) symbolisent la durée de survie (la médiane par exemple). La partie du haut suggère que le traitement augmente la durée de survie en la multipliant par Ψ. La flèche grise symbolise le temps moyen avant progression (et donc crossover). Sur la 3 ème ligne la flèche verte symbolise le temps passé avec le traitement évalué (après crossover) et donc durant lequel ces patients du groupe contrôle bénéficient de l’augmentation de survie Ψ du au traitement évalué. Après correction (4 ème ligne la flèche bleue symbolise le temps de survie qu’aurait du avoir ces patients s’ils étaient restés avec le traitement contrôle, obtenu par le calcul de correction.
Se pose alors la question d’estimer Ψ, qui correspond en partie à l’effet sur la mortalité que l’essai cherche à estimer. Seulement en partie, car l’essai cherche à estimer l’effet apporté par le traitement à partir de son instauration, tandis que ce coefficient Ψ correspond à l’effet sur la survie après progression. Il n’est pas certain que ce soit la même valeur (il est fréquent de trouver des hazard ratio différents entre les essais de 1 ère et de 2 ème ligne pour la même molécule). Cependant en pratique ce coefficient Ψ ne peut pas être estimé directement (en raison de la petitesse des effectifs des progressions). A la place soit une valeur arbitraire est utilisée (empêchant toute démonstration), soit c’est l’estimation de l’effet du traitement avant progression qui est utilisée.
Différentes méthodes de correction basées sur différentes approches ont été proposées. Le Tableau 1 les listes sans rentrer dans les détails. Le lecteur intéressé pourra aussi se référer à différents articles de synthèse. [7, 8, 9, 10, 11].
Tableau 1 – Les différentes méthodes de correction des conséquences des crossovers proposées dans la littérature
|
Exemple.
L’essai DECISION [1] a évalué le sorafenib versus placebo dans le cancer de la thyroïde. Une grande majorité des patients du groupe placebo (75%) ont fait un cross over. En ITT, une différence non statistiquement significative est obtenue au niveau de l’OS (hazard ratio 0.80, IC 95% entre 0.54 et 1.19), ne permettant pas de conclure à un bénéfice en survie du sorafenib. Dans une analyse secondaire [12, 13], reconnue d’emblée comme exploratoire, une correction de ce résultat a été tentée à l’aide de 2 méthodes : iterative parameter estimation (IPE) et rank preserving structural failure time (RPSFT). Les intervalles de confiances obtenus sont alors en faveur d’un plus grand effet traitement, devenant nominalement significatifs : IPE : 0.70-0.80; RPSFT: 0.61-0.77 avec en ITT 0.80-0.88. Compte tenu des limites de ces méthodes (cf. supra) ces résultats, comme mentionnés dans la publication, ne peuvent être considérés que comme exploratoires et ne permettent pas de conclure au bénéfice du sorafenib en termes d’OS
[3] En fait, ces méthodes ne raisonnent pas en termes de temps de survie, mais plutôt en termes de risque instantané de décès, ou de rang et nécessitent de longs développements mathématiques.