1.1 Différentes approches de « personnalisation » des traitements
1.2 Le risque de la personnalisation
1.3 L’hétérogénéité des effets traitements
4 L’évaluation des marqueurs prédictifs
5 La personnalisation sur le risque de base
7 L’évaluation de l’utilité clinique par les essais de stratégie
Le postulat de base de la médecine personnalisée est qu’il existe une hétérogénéité des effets traitement individuels. De nombreuses observations empiriques d’une apparente variabilité de « réponse » aux traitements semblent aller dans ce sens.
“The beneficial effects of most treatments vary across individuals. For example, a treatment that reduces mortality from severe COVID-19 saves some patients who would otherwise have died, but others may die despite treatment, others may survive regardless of treatment, and others may die because of adverse effects of the treatment” [19]
“In clinical practice some patients benefit more than average from treatment, whereas others do not or may even be harmed” [20]
Ces « réponses » variables d’un patient à l’autre sont, par exemple, des baisses différentes de la pression artérielle avec la même dose d’un antihypertenseur, la survenue d’un évènement cardiovasculaire ischémique chez des patients et pas chez d’autres malgré l’usage d’un antiagrégant plaquettaire ou la survenue d’une hémorragie majeure que chez certains patients.
Cependant ces constats ne permettent pas de conclure de facto à une variabilité inter-sujets du bénéfice du traitement, car ces observations peuvent avoir bien d’autres causes [19 , 21] .
Même s’il est effectivement raisonnable de postuler que l’efficacité des traitements peut être modulée par certains facteurs, au cas par cas, ce type d’observations empiriques ne permet pas de conclure à cette variabilité de l’effet traitement, car cette variabilité de « réponse » peut provenir de tout autre chose que d’une véritable variabilité individuelle de l’effet des traitements [22 , 23 , 24] . Il y a confusion entre deux concepts différents : le devenir du patient (l’outcome) et ce qu’a causé réellement le traitement dans ce devenir (l’effet causal du traitement).
Ces « réponses » que l’on peut observer au niveau individuel dans les bras traités des essais cliniques, ou dans la pratique courante, découlent de l’évolution d’un critère de jugement au cours du temps chez des patients traités. De nombreuses sources de variabilités affectent le devenir des patients (ou l’évolution de leur état). Par exemple un paramètre physiologique comme la pression artérielle est soumis à une variabilité interindividuelle, intra-individuelle, aux effets traitements. Chacune de ces variabilités conduira à des valeurs différentes de PA après l’instauration du traitement entre les sujets même si ce traitement a eu le même effet chez tous (cf. Figure 1). Rien que la variabilité intra-individuelle autour d’une valeur centrale peut faire qu’un de ces sujets a au moment de la mesure une valeur plus élevée que sa valeur centrale et un autre plus bas.
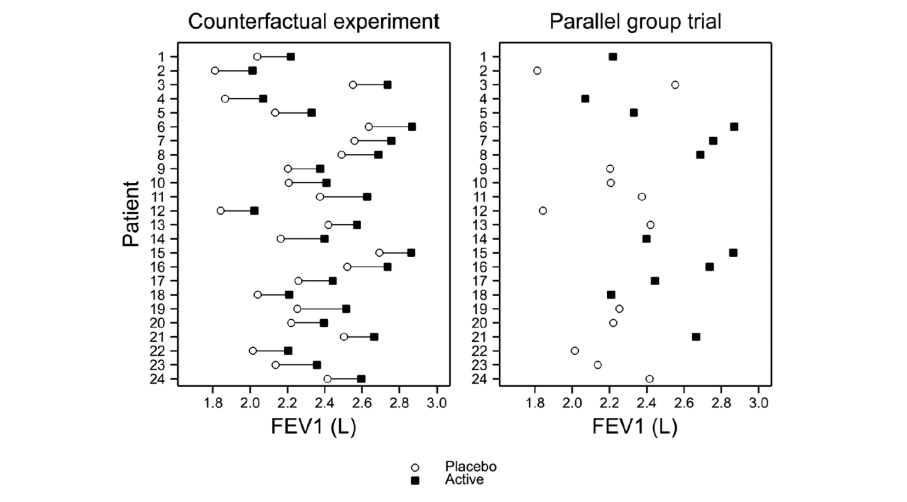
Figure 1 – Les résultats observés dans le groupe traité de l’essai (partie droite de la figure, carrés pleins) pourraient faire penser à une variabilité de la réponse VEMS des patients traités. Mais cette variabilité n’est que le reflet (partie gauche de la figure) de la variabilité intersujet de la valeur de base du VEMS, que la variabilité des VEMS dans le groupe placebo laisse aussi entrevoir. Emprunté à Senn [25] .
L’utilisation d’un changement avant-après prendra en compte la variabilité inter-sujets, mais continuera à être affecté par les autres sources de variabilités (régression à la moyenne, évolution naturelle, traitement concomitant, etc.).
L’identification de différences entre les patients, dans la réponse à un traitement demande au minimum un design randomisé en multiple cross-over afin de prendre en compte la variabilité inter-sujets à l’aide de la randomisation et la variabilité intra-sujets à l’aide de la répétition des périodes de traitement [26] (cf. aussi la figure 213 du supplément 2 du papier décrit ci-dessous).
Ce design a été utilisé pour montrer une hétérogénéité de réponse à 4 traitements antihypertenseurs [27] . Pour objectiver une variabilité de réponse dans la pression artérielle systolique entre les sujets, chaque patient recevait les 4 traitements dans un ordre aléatoire avec 2 traitements répétés 2 fois (soit 6 périodes de traitement de 7 à 9 semaines par patient). Une hétérogénéité de réponse des patients aux traitements a été mise en évidence avec en moyenne une différence de 4.4mmHg entre le meilleur traitement pour un patient et les autres traitements. Si ces résultats sont confirmés, ils plaideront potentiellement pour une personnalisation du choix du traitement antihypertenseur. En pratique cette personnalisation pourra passer par la réalisation d’essai de taille 1 (N-of-1) (cf. chapitre 22). Cette perspective nécessite cependant de discuter si une optimisation de la baisse de pression artérielle laisse aussi présager d’une optimisation en termes de prévention des évènements cliniques, ce qui débouche sur la question de la valeur de surrogacy de la baisse de pression artérielle et des bénéfices accessoires des différentes classes pharmacologiques d’antihypertenseur.
Pour les événements cliniques, il n’y a pas de notion de variabilité intra-individuelle. Les évènements cardiovasculaires surviennent spontanément de façon erratique chez des patients pourtant très comparables cliniquement, sans que l’on puisse identifier le ou les déterminants de leur déclenchement. La survenue des évènements indésirables, même très pathognomoniques, pour lesquels le médicament est indéniablement la cause, ne survient pas chez tous les patients, sans que l’on comprenne bien souvent la raison.
Devant cette variabilité irréductible et non inexplicable, les modèles statistiques s’imposent, car ils permettent de modéliser cette variabilité de manière satisfaisante. Car, même si les sujets sont différents entre eux, il y a une assez bonne stabilité, d’un grand groupe de sujets à l’autre, des paramètres statistiques comme la moyenne, la distribution des valeurs, la fréquence, la moyenne des temps de survenue des évènements, etc. Les prédictions faites sur les groupes de sujets sont plus souvent fiables que celle faite au niveau des individus.
Ainsi, à l’exception des essais n-of-1 (qui ne s’appliquent pas si le critère de jugement est un événement), l’observation de l’effet traitement individuel (ITE , Individual Treatment Effect ) est impossible, car cela nécessiterait de connaitre le contrefait, c’est-à-dire ce que serait devenu le patient sans traitement [19 , 28] . Le constat d’une variabilité des états et des évolutions des patients sous traitement ne permettent pas de conclure que le traitement a eu des effets différents d’un patient à l’autre.
L’effet du traitement sur un patient particulier est non observable
De ce fait, il est impossible de vraiment personnaliser les effets des traitements et il est donc impossible de faire une véritable médecine personnalisée, au sens strict du terme, basée sur la connaissance de ce qu’apporterait un traitement à un patient donné.
Par contre il est possible de déterminer l’effet moyen d’un traitement (ATE , Average Treatment Effect ), à l’aide d’un essai randomisé (ou une étude observationnelle recevable pour une inférence causale) [29 , 30 , 31 , 32] . L’effet moyen sous-entend l’homogénéité de cet effet à travers la diversité des patients inclus dans l’étude.
Dans ce cadre il est cependant possible de chercher des facteurs qui pourraient modifier l’effet traitement moyen par différentes approches comme l’analyse en sous-groupes (analyse stratifiée) ou la modélisation. Cela introduit le concept de cATE (conditional Average Treatment Effect ) dans le raisonnement : l’effet du traitement ne peut être inféré (estimé) de manière causale que par un effet moyen sur un groupe de sujets (ATE) ; mais cet effet moyen est recherché de manière plus fine en fonction des facteurs qui conditionnent sa valeur (d’où le conditional ).
L’idée est finalement la même que celle de la médecine personnalisée, identifier les situations où un traitement est plus ou moins adapté aux patients, mais, contrairement à la personnalisation stricto sensu, cette approche est faisable. Il a été proposé de nommer cette approche « médecine stratifiée » compte tenu de son cadre analytique. Dans le langage courant, la distinction entre les termes de médecine stratifiée et médecine personnalisée est rarement faite et le terme médecine personnalisée s’est imposée certainement en vertu de sa valeur marketing.
Ces notions d’inférence causale, en particulier celle que l’effet traitement est non observable chez un patient donné, déclenchent souvent des discussions impétueuses entre statisticiens et cliniciens.
L’exercice clinique ne peut se faire qu’en raisonnant au niveau des cas isolément. Pour un clinicien, le champ d’observation naturel est un individu, puis un autre, etc. Il doit solutionner le problème d’un patient par les décisions et actions qu’il prendra pour ce patient. Le seul retour de ses actions qu’il aura sera l’observation empirique, chronologique, de l’évolution de l’état du patient. Dans ce cadre, il est évident que, naturellement, du fait de son expérience sensible, on associe l’évolution du patient à la conséquence de ces décisions, actions (en particulier les traitements apportés), même si d’ailleurs on sait parfaitement que cette évolution peut être conditionnée par beaucoup d’autres facteurs non appréhendables.
Il y a donc opposition entre la conceptualisation empirique que fait le clinicien de son expérience sensible et sa conceptualisation des problématiques liées à la variabilité du vivant qui relève du champ de la pensée et de l’abstraction. La pratique médicale est de l’ordre de l’expérience sensible, mais pour appréhender les conséquences de la variabilité du vivant sur cette expérience sensible on doit faire appel aux champs de la pensée et de l’abstraction. Et il est naturel que ces 2 niveaux se heurtent farouchement entre eux, en particulier dans l’instantanéité de l’action.
Ce qui complique encore plus la perception de ces deux niveaux est qu’il existe des effets parfaitement déterministes en médecine, perceptibles par l’expérience sensible, comme les effets toxiques ou des effets pharmacologiques intenses (curares, anesthésiques généraux).
Au niveau individuel, l’incertitude liée à la variabilité du vivant est très difficile à prendre en compte, car dans ce cadre notre cerveau ne gère pas naturellement l’incertitude. Ainsi le facteur de risque devient cause révélée après l’infarctus du myocarde, même si l’élévation du LDL n’augmente que de quelques pourcents le risque d’infarctus. Pour un patient sous statine, la survenue d’un infarctus devient un échec patent de la molécule, même si ce traitement ne fait que réduire, sans l’annuler, le risque d’infarctus. Dans ce cadre, peut-être pour des raisons psychologiques, sociétales, culturelles, il nous semble nécessaire de connaitre la cause, la raison de l’évènement, et même si notre réflexion, en dehors de l’investissement dans un cas particulier, conceptualise très bien l’incertitude qu’il existe dans cette démarche.