2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
17.1 Déplétion des susceptibles
17.2 Biais lié à un défaut de synchronisation des t0
17.3 Groupe contrôle externe non-traité
17.5 Le biais de sélection vu en termes statistiques : censure à gauche, censure à droite
18 Identifications des patients dans la source de données
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
La question du temps zéro (t0) de début de suivi des patients est une question cruciale pour un groupe contrôle externe (voir aussi la section 18.1.1). De la justesse de sa définition et de sa similitude avec celui du groupe traité dépendra directement la validité des résultats produits. Sur ce point aussi, l’émulation d’un essai cible permet d’éviter les bévues [185] .
Suissa et al. montre que dans une comparaissons à un groupe contrôle externe d’une étude monobras du blinatumomab dans la leucémie aigüe lymphoblastique réfractaire ou en rechute, le choix du t0 conduit à des résultats soit en faveur d’un bénéfice soit non concluants [186] .
Dans les études expérimentales (essais randomisés, études monobras) le début du suivi (t0) correspond à un instant où :
Dans ces études, cet instant est parfaitement bien défini et parfaitement bien identifiable dans le fichier de données. Toute la difficulté va être de synchroniser le t0 du début du suivi des patients dans le groupe contrôle externe avec celui du groupe traité.
Cette synchronisation des t0 est indispensable pour éviter les biais, en particulier le biais par temps d’immortalité. L’exemple suivant illustre le mécanisme des biais qui peuvent être induits en cas de mauvaise synchronisation des t0 entre le groupe traité et le groupe contrôle externe.
Dans une hémopathie maligne, un nouvel anticorps bispécifique a la même cible qu’un CART-T cells utilisé en standard. Le groupe traité est représenté par une étude monobras de cet anticorps bispécifique (il s’avérait impossible de financer un essai comparatif compte tenu du coût du CART T cells). Une comparaison externe avec un groupe contrôle recevant le CAR-T cells est envisagé.
Le groupe contrôle est extrait d’un registre de patients ayant bénéficié d’un CAR-T cells. Une particularité du traitement par un CAR-T cell est qu’il s’écoule un délai entre la décision de recourir à ce traitement et le moment où le traitement est prêt pour être administré. Ce délai est le temps nécessaire pour réaliser la leucaphérèse et la transformation des cellules avant leur injection aux patients. Il s’avère que certains patients vont malheureusement décéder durant cet intervalle ou progresser ou ne plus être éligible à l’administration du traitement en raison d’une dégradation de leur état général. Il arrive aussi que la préparation des cellules échoue. Ces patients n’ayant pas reçu le traitement n’apparaitront pas dans le registre constitué de patients ayant reçu un CAR-T cells. Pourtant ces mêmes patients, s’ils avaient été inclus dans l’étude monobras, auraient été comptabilisés et leur devenir pris en compte pour les critères de jugement (survie sans progression, survie globale).
Ainsi, la comparaison à ce registre introduira un biais lié au t0 (si le début du suivi ne commence pas au même moment dans les 2 groupes, des événements ne seront pas observés dans le groupe contrôle leur qu’ils l’auraient été dans le groupe traité) et à un temps d’immortalité si l’analyse fait débuter le suivi des 2 groupes au diagnostic afin d’avoir le même t0 dans les 2 groupes (dans ce cas aucun événement ne sera observé durant la première partie du suivi des patients CART-cell, correspondant au temps de préparation du traitement, comme si les patients étaient « immortels » initialement).
Le recours à l’émulation d’un essai cible (cf. section 22) permet de comprendre ces 2 phénomènes. Dans un essai randomisé où l’anticorps bispécifique aurait été directement comparé au CAR-T cells, le suivi des patients aurait débuté dès la randomisation dans les 2 groupes et non pas à l’administration dans le bras CAR-T cells. Les progressions et décès avant administration auraient été pris en compte dans ce bras (tout comme les mêmes événements précoces survenant dans le bras bispécifique). De plus, l’essai cible aurait été analysé en intention de traiter et les patients alloués au bras CAR-T cell qui n’aurait pas pu recevoir l’injection du traitement aurait été maintenu dans le bras et l’analyse (avec leurs événements) tandis qu’ils ont tout bonnement disparu du registre et donc du bras contrôle externe.
Pour éviter ces biais il serait nécessaire d’avoir dans la source de données servant à constituer le groupe contrôle tous les patients pour lesquels l’indication de CAR-T cells a été portée (qu’ils aient pu ou non-recevoir ensuite l’injection du traitement). Cela nécessite donc d’avoir un registre de pathologie plutôt que traitement, où les données des décisions de traitement sont collectées, par exemple, avec la présence des comptes rendus des réunions de concertation pluridisciplinaire. En pratique il s’avère fréquemment que les informations indispensables pour émuler correctement un essai cible et éviter ces biais ne sont pas disponibles dans les sources de données, car ce besoin n’a pas été anticipé. Cela renvoie à la nécessité que le recueil des données dans les sources de données mobilisables pour ce type d’études soit construit après une réflexion concernant leurs usages (cf. section 20.6)
L’évaluation d’un nouveau traitement dans un essai randomisé de supériorité repose sur l’analyse en intention de traiter. En termes d’émulation cela nécessite que le suivi dans le groupe contrôle externe débute dès l’assignement du traitement au patient, effectué immédiatement après la vérification de l’éligibilité. L’événement le plus proche de cela dans les données observationnelles est la prescription du traitement par le médecin. Dans le cas de traitement non médicamenteux, cette prescription correspond à la décision (du médecin ou collégiale dans une RCP) de proposer une certaine stratégie thérapeutique (chirurgie, intervention, CAR T cell, etc.) au patient. La date de prescription (ou de décision de recourir à un certain traitement) permet ainsi une émulation satisfaisante de l’analyse en ITT.
Temps d’immortalité - définition
Le temps immortel est une période de suivi prise en considération dans l’analyse, mais où par construction un patient ne peut pas présenter l’événement d’intérêt, car les patients qui ont présenté l’événement durant cette période ont été exclus par construction de l’étude.
Par exemple dans le cadre d’un traitement en prévention primaire, la sélection dans le groupe traité de patient ayant eu au moins 6 mois de traitement entrainera qu’aucun événement ne pourra survenir durant ces 6 mois. En effet si un événement moins de 6 mois après l’instauration du traitement, celui-ci devient non éligible. Si bien que l’éligibilité dans ce groupe devient : avoir initié un traitement de prévention primaire et ne pas avoir fait d’événements d’intérêts avant 6 mois. Comme le suivi de ces patients débute à l’initiation du traitement, aucun événement ne surviendra durant les 6 premiers mois du suivi, ces 6 premiers mois seront un temps immortel.
NB : si la question clinique d’intérêt est une comparaison de durées de traitement, les groupes devront être constitués sur la base de la durée de la prescription initiale et non sur la durée effectuée. Si la prescription ne précise pas la durée anticipée, la réponse à cette question devra faire appel à une tout autre approche. [187] . À noter cependant que la question de l’évolution de l’effet traitement au cours du temps est une question exploratoire ne correspondant pas à un estimand causal d’évaluation de l’intérêt clinique de la prescription d’un traitement.
La disponibilité de cette date dans la source de données utilisée pour le groupe contrôle n’est pas garantie. Elle sera très certainement absence dans une base administrative où seulement la date de dispensation du traitement sera présente. Elle peut ne pas être présente aussi dans des sources de données orientées recherche comme des registres. Si les données sont extraites de dossiers médicaux, celle-ci pourra être extraite des dates des ordonnances, des lettres de liaison, de prise de rendez-vous auprès du service allant appliquer le traitement (chirurgie, radiothérapie, etc.) ou des comptes rendus de réunion de concertation pluridisciplinaires (RCP) lors de la phase d’abstraction/extraction des données (manuelle ou automatique, spécifique à l’étude ou non). La prise de conscience de ce point par les gestionnaires de données est indispensable pour augmenter l’utilisabilité des sources de données qui se constituent pour ce type d’étude (cf. section 20.6).
Il faut aussi que le suivi pour le groupe traité débute lui aussi au moment de la décision d’utiliser le nouveau traitement (date d’inclusion dans une monobras ou date de randomisation).
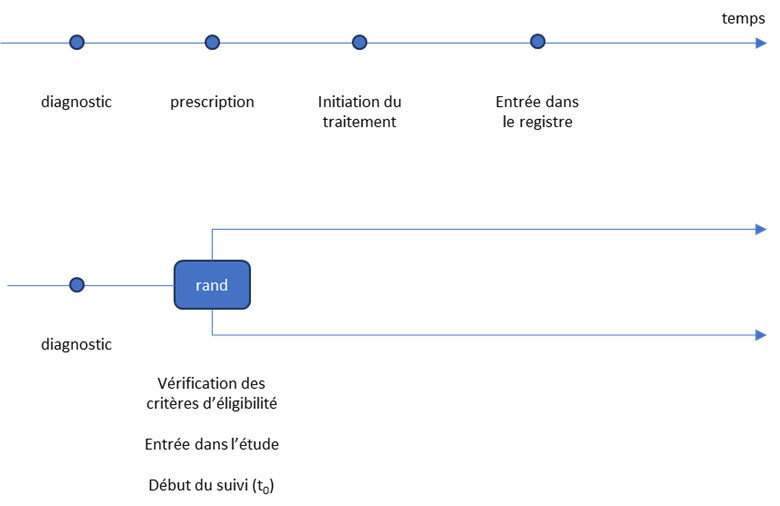
Figure 15 – Comparaison de la chronologie des événements entre un essai randomisé (en bas) et un recueil de données de routine (en haut).
Dans certains cas, la date de début de traitement peut être employée comme t0 du groupe contrôle sans trop de risque de biais de sélection, par exemple quand il est raisonnable de penser que le traitement a été débuté très peu de temps après la prescription et/ou quand il est peu probable que des événements critère de jugement puissent survenir dans cet intervalle.
Dans tous les cas, la réflexion par rapport à ce qui se passerait dans un essai randomisé équivalent (évaluation d’essai cible) réduit le risque de défaut de conception conduisant à un biais de ce type (cf. section 22).
Situations pouvant créer un biais de sélection :
La granularité temporelle doit être suffisamment fine pour éviter une reverse causation liée à une mesure de l’association de type transversale et non pas longitudinale. En effet, les dates des événements, des mesures, des examens ou des traitements ne sont parfois pas directement connues (colligées) mais dérivées des dates des comptes rendus de consultations, de visites pour les registres, d’hospitalisations, etc. Cette incertitude temporelle peut très bien conduire à considérer que deux informations sont séparées dans le temps alors, qu’en réalité, elles étaient synchrones, ou même, de temporalité inverse.
Un délai de grâce est parfois proposé comme solution à un éventuel biais par temps immortel dans les études observationnelles classiques. Cette solution n’est pas vraiment adaptée aux groupes contrôles externes, car elle conduirait à tronquer aussi le suivi du groupe traité issu d’une monobras ou d’un essai randomisé.