2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
6.1 Le manque de fiabilité des études observationnelles
6.2 Des études montrant des associations, mais ne permettant pas de conclure à la causalité
6.3 Différences avec les études de pharmacoépidémiologie
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
Jusqu’à très récemment, les études observationnelles étaient considérées comme insuffisamment fiables pour répondre à des questions d’efficacité des traitements [21] [22] [23] [24] [25] . Ceci reposait sur l’existence de problématiques méthodologiques jusqu’à présent insolubles [26] et sur de très nombreux exemples où l’efficacité de traitements mis en évidence par des études observationnelles avait été ensuite infirmée par des essais randomisés de confirmation (cf. encadrés).
Traitement hormonal substitutif de la ménopause (THSM) et prévention des événements cardiovasculaires – L’étude observationnelle de la Nurses’ study montrait que l’utilisation du THSM était associée avec une moindre fréquence des événements cardiovasculaires par rapport aux femmes ne l’utilisant pas [27] . L’essai randomisé WHI versus placebo a mis en évidence que le THMS causé une augmentation des événements cardiovasculaires de xx% [28] . Cet exemple fût un des premiers objectivant la possibilité d’obtenir des résultats faussement positifs sur l’efficacité des traitements avec les études observationnelles et a fortement contribué à la mise en évidence des limites de ces études pour cet usage [29] .
Sémaglutide et prévention de la maladie d’Alzheimer – Deux essais randomisés ont échoué note n° 7 à montrer que le sémaglutide permettait de prévenir la maladie d’Alzheimer (EVOKE NCT04777396 et EVOKE+ NCT04777409 [30] ). Ces essais ont été entrepris sur la base de 2 études observationnelles montrant un bénéfice potentiel. Une de ces études était construite suivant le cadre de l’émulation d’un essai cible. Malgré cela il est probable que cette étude ait conduit à des résultats biaisés en raison d’un biais de temps d’immortalité comme le témoignent les courbes d’incidences cumulées de la figure rapportées dans la publication [31] .
Des études méta-épidémiologiques [32] [33] [34] [35] mettent en évidence ce manque de fiabilité des études observationnelles et le risque encouru de conclure faussement à l’efficacité des traitements. Les études observationnelles de haute qualité peuvent donner des estimations proches de celle des essais randomisés, mais pas de façon systématique, obérant ainsi la possibilité d’en faire un outil standard d’évaluation des bénéfices cliniques [36] [37] .
Ces observations, et les réticences qui en découlent, concernent principalement les études observationnelles « classiques », mais peuvent naturellement être étendues aux comparaisons externes qui ne sont qu’un type particulier d’études observationnelles sur l’efficacité des traitements.
On commence d’ailleurs à observer des discordances similaires entre des comparaisons à un groupe contrôle externe et un essai randomisé évaluant tous les deux le même traitement versus le même contrôle dans des situations cliniques similaires (cf. exemple de l’idecabtagene vicleucel ci-dessous).
Le CAR T cell idecabtagene vicleucel (Abecma) n’a fait l’objet que d’une étude monobras dans le traitement du myélome multiple réfractaire ou en rechute (RRMM) en 4 ème ligne ou plus (L4+). Une comparaison au standard of care a été effectuée à l’aide d’un groupe contrôle externe et elle montre un bénéfice clinique important du CAR T cell par rapport aux traitements standards en termes de survie globale. Cette comparaison n’a pas été publiée et elle n’est disponible que dans l’EPAR du produit (Figure 28 page 97) [38] .
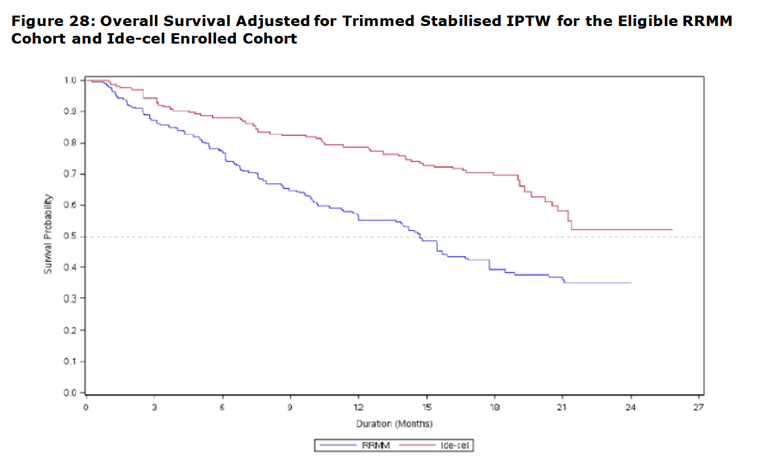
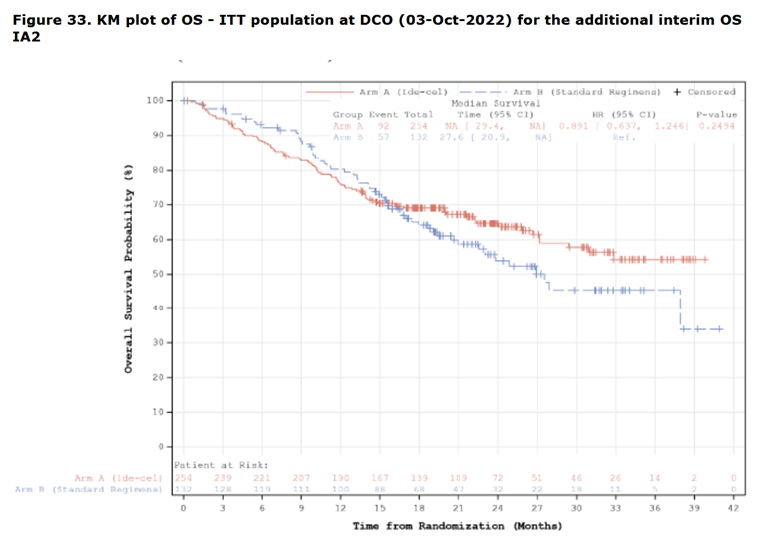
Ultérieurement un essai randomisé effectuant la même comparaison chez des patients légèrement différents (2ème ligne ou plus) n’a pas mis en évidence de bénéfice du CAR T celle par rapport au traitement standard. (EPAR variation [39] ).
Le résultat de la comparaison externe s’avère donc très discordant par rapport à celui de l’essai randomisé amenant à s’interroger sur sa fiabilité.
Pour l’instant il n’existe un nombre réduit d’études méta-épidémiologiques de validité empirique des comparaisons externes, principalement parce que les essais randomisés de confirmation ne sont pas réalisés (cf. section 28.2).
[7] https://ml-eu.globenewswire.com/Resource/Download/1328a3cb-6359-4bb8-aef1-c7eab58d3016