3.2 Évaluation clinique des thérapies ciblées
3.3 Utilisation d’essais non comparatifs
3.4 Efficience globale des traitements ciblés
4 L’évaluation des marqueurs prédictifs
5 La personnalisation sur le risque de base
7 L’évaluation de l’utilité clinique par les essais de stratégie
Les essais cliniques nécessaires pour démontrer le bénéfice clinique de ces molécules ciblées sont tout à fait classiques. La présence de la variante est un des critères de sélection de l’essai qui n’inclue que des patients présentant cette variante (patients marqueur positif) :
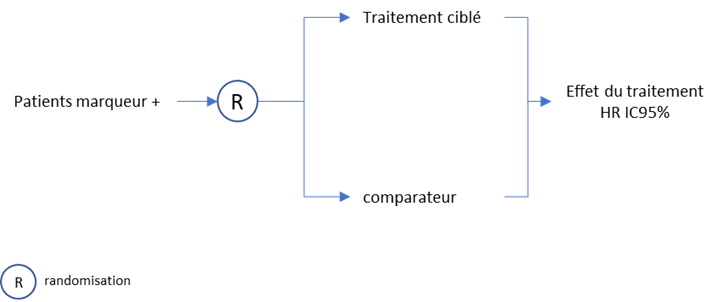
L’essai FLAURA [40] a évalué l’osimertinib versus un TKI de référence (gefitinib ou erlotinib) en première ligne du traitement du cancer du poumon non à petite cellule avancé. Pour être inclus dans cet essai, les patients devaient présenter une mutation de l’EGFR (exon 19 deletion ou L858R allele). La méthodologie de l’essai est classique : essais randomisés en 2 bras parallèles, sans double aveugle, avec la PFS et l’OS comme critère de jugement décisionnels. Cet essai a démontré la supériorité de l’osimertinib chez ces patients en termes de survie.
En effet, ici, le but de l’évaluation clinique n’est pas d’établir l’intérêt de la variant moélculaire pour choisir parmi différentes options dans la thérapeutique de la pathologie, mais de démontrer le bénéfice clinique de la molécule chez les patients présentant cette altération moléculaire. Il s’agit d’un parti pris de développement et l’évaluation clinique porte sur le couple molécule et présence de la cible simultanément. Par principe il est considéré que la molécule ne peut apporter aucun bénéfice chez les patients non porteurs de l’altération moléculaire note n° 7 .
La situation est donc complètement différente de celle où un biomarqueur prédictif (modificateur de l’effet) est recherché pour une molécule qui a déjà démontré un bénéfice chez des sujets tout-venant (« all comers »)
[7] Ce qui est une hypothèse forte, car l’affinité de ces molécules peut ne pas être nulle pour les autres variants de la cible.