4 L’évaluation des marqueurs prédictifs
5 La personnalisation sur le risque de base
5.1 Variation du bénéfice absolu en fonction du risque de base
5.2 Mise en application pour personnaliser les traitements
5.3 Évaluation clinique d’une personnalisation sur le risque
5.3.1 Performance d’un outil de prédiction
5.4 L’évaluation de l’utilité clinique
7 L’évaluation de l’utilité clinique par les essais de stratégie
L’évaluation de l’utilité clinique des personnalisations basée sur le risque de base s’effectue principalement à l’aide d’un essai de stratégie en non-infériorité. Le but est, en premier lieu, de montrer qu’il n’y a pas de perte de bénéfice par rapport au traitement de tous les patients, d’où l’approche de non-infériorité. L’essai devra aussi montrer que la personnalisation s’accompagne bien de l’avantage recherché, comme la réduction des effets indésirables, et qu’il y a donc un intérêt patent à ne pas traiter tous les patients. La principale difficulté de cette évaluation réside dans le choix de la limite de non-infériorité.
L’essai DYNAMIC [93] a évalué l’intérêt clinique de l’ADN circulant pour guider le choix du traitement adjuvant dans le cancer du côlon au stade II.
À ce stade une chimiothérapie adjuvante (à base d’oxaliplatine ou par fluoropyrimidines) peut être proposée après la chirurgie. Compte tenu du bon pronostic à ce stade, de l’incertitude sur un réel bénéfice sur la mortalité de la chimiothérapie adjuvante et des effets secondaires de celle-ci, la balance bénéfice risque de cette chimiothérapie adjuvante reste débattue. D’où la question d’envisager une désescalade thérapeutique chez les patients ayant le plus faible risque, en ne leur proposant pas de chimiothérapie. Sur le plan de l’évaluation, le but de cette désescalade est de diminuer la proportion des patients ayant des effets indésirables, sans pour autant perdre en efficacité, c’est-à-dire sans augmentation de la fréquence des récidives par rapport à la prise en charge actuelle de ces patients. L’ADN circulant (ADNc, biopsie liquide) représente une piste pour guider cette désescalade en ne réservant la chimiothérapie qu’en cas de résultat positif 4 ou 7 semaines après la chirurgie.
Cet essai a donc comparé une stratégie basée sur l’ADN circulant (ADNc) par rapport à la stratégie habituelle. Le critère de jugement, classique en situation adjuvante, était la survie sans récidive (RFS) à 2 ans. L’essai était un essai de non-infériorité afin de montrer que le bras désescalade n’entrainait pas une perte de chance trop importante par rapport à la stratégie actuelle.
Au premier abord, cet essai semble donc parfaitement adapté à son objectif et à même d’apporter une réponse de haut niveau de preuve. Cependant, plusieurs limites méthodologiques apparaissent à la lecture approfondie de cet article.
Dans l’essai de non-infériorité les biais marchent à l’envers de ceux de l’essai de supériorité : sera cause de biais tout ce qui contribue à réduire la différence existante entre les 2 groupes et qui conduit à ne pas pouvoir mettre en évidence que le nouveau traitement est en réalité inférieur au traitement standard. Cette situation survient, entre autres, lorsque les deux groupes ne reçoivent pas les traitements de l’étude. Dans ce cas, le critère de jugement dépendra uniquement du risque de base des patients inclus dans l’essai et sera identique entre les 2 groupes conduisant à conclure automatiquement à la non-infériorité. Cette situation est caricaturale, mais permet de bien comprendre le primum movens de la problématique.
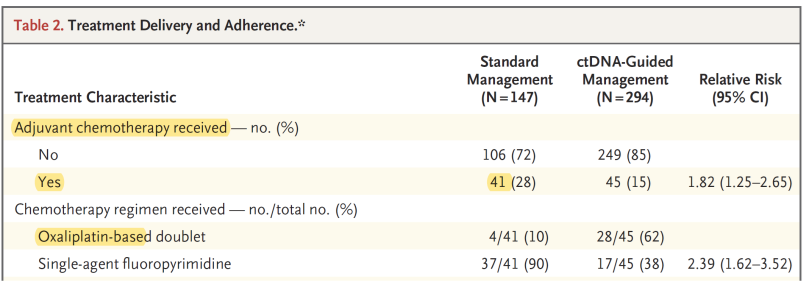
Dans cet essai, seulement 28% et 15% des patients, respectivement des groupes "stratégie classique" et "stratégie basée" sur l’ADNc, on reçut un traitement adjuvant (cf. table 2 de l’article). Même si la stratégie ADNc prive à tort de traitement adjuvant des patients à risque de récidive, les taux de récidive (RFS) de ces 2 groupes seront très proches, car la majorité des patients de ces 2 groupes ne reçoivent pas de traitement adjuvant de toute façon (décision basée principalement sur la clinique).
En effet, si la stratégie ADNc est inférieure et augmente le nombre de récidives ou de décès, car elle prive de chimiothérapie des patients à haut risque contrairement à l’approche classique, le surcroit de récidives que cause cette stratégie ne concernera qu’au maximum 13% des patients (28% - 15% = 13%). Cette différence sera alors diluée par les patients pour lesquels rien n’est différent entre les 2 groupes et qui sont majoritaires. Ainsi, la conclusion à la non-infériorité est quasiment assurée même en cas de nette infériorité du fait de cette dilution.
Pour éviter cette problématique, il aurait fallu inclure des sujets pour lesquels l’approche actuelle implique le traitement adjuvant et les randomiser entre un groupe où ce traitement est appliqué et un groupe où l’indication du traitement adjuvant est réévaluée à l’aide du ADNc. Cette approche permet de répondre à la question : chez des patients qui actuellement recevraient un traitement adjuvant, l’ADNc permet-il d’identifier ceux chez lesquels il est en réalité inutile ?
Une autre interrogation survient avec l’analyse de la limite de non-infériorité utilisée. Celle-ci est de 8.5% en termes de différence de RFS à 2 ans. La stratégie ADNc sera considérée comme non-inférieure tant qu’elle n’entrainera pas une augmentation de plus de 8.5% du taux de récidive à 2 ans (ou une diminution de 8.5% de la RFS).
Pour évaluer l’acceptabilité des limites de non-infériorité, il est nécessaire de se référer à l’efficacité du comparateur afin de déterminer la limite maximale acceptable, qui correspond à la perte de 100% de l’apport du traitement standard. Une méta-analyse Cochrane du traitement adjuvant au stade 2 est disponible note n° 20 et donne un risque ratio de 0.83 (IC 95% entre 0.75 et 0.92). Dans le contexte de cet essai, la RFS dans le groupe standard est de 92.4% correspondant à un risque de récidives ou décès de 7.6%. Dans ce contexte, l’effet du traitement adjuvant en termes de différence des risques (ARR) peut être estimé à (1 – 1/0.92) * 7.6%, soit 0.66%, montrant que la limité utilisée est excessivement tolérante.
Dans ces essais de désescalade, s’assurer que réduire le traitement n’entraine pas une perte de chance rédhibitoire par une logique de non-infériorité est indispensable, mais ce n’est pas la seule démonstration à apporter. Il convient aussi de montrer que cette désescalade s’accompagne bien d’un bénéfice pour le patient, au niveau des effets indésirables. Dans cet essai, cet objectif n’est pas abordé directement. Seule la fréquence de recours à un traitement adjuvant est mesurée et met en évidence la moindre utilisation déjà citée : 28% versus 15% (cf. table 2 de l’article ci-dessous). Cependant, dans le groupe ADNc, les investigateurs choisissent plus fréquemment en cas de positivité du ADNc un traitement adjuvant à base d’oxaliplatine, de moins bonne tolérance qu’une monothérapie avec une fluoropyrimidine. Ce résultat interroge vraiment sur l’obtention du but recherché avec la désescalade.
Une tout autre approche aurait pu être envisagée : ADNc ne permettrait-il pas de trouver des sujets qui bénéficieraient du traitement adjuvant alors qu’ils ne sont pas identifiés par l’approche classique ? Pour le montrer, des patients sans indication de traitement adjuvant avec la stratégie actuelle seraient alors randomisés entre un groupe contrôle et un groupe expérimental où un traitement adjuvant serait quand même mis en place en cas d’ADNc positif afin de montrer la supériorité de l’approche basée sur l’ADNc.
Lorsque l’objectif est d’éviter d’exposer tous les patients à la toxicité du traitement, une approche de bénéfice net en supériorité est aussi envisageable à la place d’une approche de non-infériorité. Elle aura pour principal intérêt d’évincer la difficulté de la fixation de la limite de non-infériorité.
Pour l’instant (juillet 2023), il n’existe que quelques autres exemples comme l’essai TAILORx [94] ou l’essai MINDACT [95] pour la décision de traitement adjuvant dans le cancer du sein précoce.
[20] Figueredo A, Coombes ME, Mukherjee S. Adjuvant Therapy for completely resected Stage II Colon Cancer. Cochrane Db Syst Rev 2008; 2010: CD005390.