4 L’évaluation des marqueurs prédictifs
5 La personnalisation sur le risque de base
7 L’évaluation de l’utilité clinique par les essais de stratégie
7.1 Principe des essais de stratégie
7.3 Exemple 2 – L’essai COAG, génotypage pour l’ajustement des doses de la warfarine
7.4 Exemple 3 – pharmacogénétique pour la prévention des effets indésirables
Les essais de stratégie ont pour objectif de démontrer l’utilité médicale des marqueurs prédictifs ou de tout autre type d’outils proposés pour prédire le bénéfice des traitements. Ils permettent de savoir si l’utilisation du marqueur prédictif dans un but décisionnel (c’est-à-dire de personnalisation des traitements) permet effectivement, en pratique, d’améliorer le devenir des patients (davantage d’évènements prévenus, moins d’effets indésirables sans perte d’efficacité, etc.) par rapport à une stratégie n’intégrant pas le marqueur (standard de soin).
Le design de ces études est représenté Figure 4. Les patients éligibles sont randomisés entre un bras « stratégie basée sur le marqueur prédictif » et un bras « stratégie habituelle ».
We conducted a randomized, open-label, assessor-blinded trial in which patients undergoing primary PCI with stent implantation were assigned in a 1:1 ratio to receive either a P2Y12 inhibitor on the basis of early CYP2C19 genetic testing (genotype-guided group ) or standard treatment with either ticagrelor or prasugrel (standard-treatment group ) for 12 months [134]
Dans le bras expérimental, le marqueur est évalué chez tous les patients et le traitement est choisi en fonction du résultat. Plusieurs variantes sont possibles à ce niveau, le choix peut se faire entre deux traitements conventionnels déjà disponibles ou entre un nouveau traitement ou une nouvelle modalité de ce traitement et le traitement conventionnel (comme le doublement de la dose de clopidogrel dans l’exemple de l’essai TAILOR-PCI développé ci-dessous).
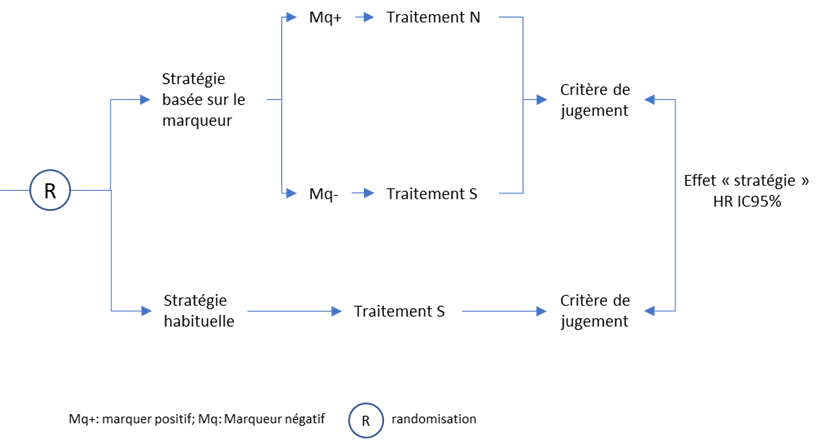
Figure 4 – Principe des essais de stratégie
De nombreuses variantes de ce design sont utilisées [16] . En particulier, se pose la question du dénominateur. La logique du design voudrait que la fréquence des évènements, calculée avec le nombre de patients randomisés dans chaque bras comme dénominateur, soit comparée globalement entre le bras expérimental et le bras contrôle. Cette analyse répond à la question « en quoi l’adoption de la stratégie de personnalisation éviterait globalement la survenue d’évènements », sur l’ensemble de la population des malades correspondants. Cependant parmi tous ces malades le bénéfice attendu ne concerne structurellement qu’une partie d’entre eux (plus ou moins importante en fonction de la prévalence de la positivité du marqueur). Une autre option d’analyse est de ne considérer dans les deux groupes que les patients marqueurs positifs et de comparer ainsi la fréquence des évènements chez les patients marqueurs positifs dans le bras expérimental versus celle dans le bras contrôle aussi uniquement chez les mêmes patients marqueurs positifs. Cette approche nécessite que le marqueur soit là aussi recherché dans le groupe contrôle mais non exploité (avec un risque de contamination intergroupe si le résultat est disponible pour les investigateurs).
Exemple – TAILOR-PCI
L’essai TAILOR-PCI [135] a comparé, après pose d’un stent coronarien, une stratégie d’adaptation de la dose du clopidogrel basée sur le génotype par rapport à la pratique habituelle d’une dose fixe. Le critère de jugement était les évènements cardiovasculaires. Le génotype recherché était les variants du gène CYP2C19*2 or *3 considérés comme des marqueurs de perte de fonction (cf. supra).
L’essai a inclus 5302 patients. L’analyse primaire préspécifiée ne portait que sur les patients porteurs des variants de perte de fonction, ce qui conduisait à exclure de l’analyse 3453 patients. L’analyse primaire porte finalement sur 1849 patients. Une analyse sur tous les patients inclus était prévue comme analyse secondaire.
L’essai échoue à montrer une réduction des évènements cardiovasculaires avec un résultat de l’analyse préspécifiée non statistiquement significatif alors que l’essai avait la puissance voulue pour mettre en évidence l’effet traitement recherché. Cet essai n’a donc pas apportée de preuve formelle de l’utilité médicale de la mise en pratique d’une stratégie basée sur le génotype du CYP2C19 dans ce contexte clinique.
D’autres essais similaires [134 , 136] ont donné des résultats comparables.