2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
18.1.1 Détermination du t0
§ Cas particulier du groupe contrôle non traité
§ Captation des patients perdus de vue
18.2 Représentation graphique du processus d’extraction des données de l’étude
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
Dans le groupe traité, où les patients sont inclus prospectivement, leur éligibilité est vérifiée à la date de la visite de sélection (des variantes existent, mais ne changent pas le schéma général décrit ici). Si le patient s’avère éligible et consent à être inclus, ses caractéristiques de baseline sont mesurées à cette visite. La date de la baseline est donc parfaitement bien définie. Souvent cette éligibilité et/ou les caractéristiques de base reposent sur une imagerie qui a pu être faite quelques jours au paravent, mais ces informations sont rattachées à cette date. La date d’inclusion, à laquelle est mesurée la baseline est donc clairement définie.
Dans la constitution d’un groupe contrôle (cohorte) à partir de données historiques, la situation est plus complexe, car il n’y a pas de visite d’inclusion [188] [189] .
Pour reproduire au mieux ce qui se passe dans un essai randomisé, le suivi devrait débuter à la date où le patient vérifie les critères d’éligibilité et reçoit une prescription note n° 22 du traitement d’intérêt [197] . Dans beaucoup de sources de données, la notion de prescription n’est pas disponible et elle sera remplacé par la dispensation ou le début du traitement. Cette approximation peut cependant introduire un biais de sélection par temps d’immortalité dans certaines situations (cf. section 17.2).
Dans une étude monobras, des patients hospitalisés pour une exacerbation de BPCO reçoivent, à la sortie de l’hôpital, un nouveau traitement dont le but est de prévenir les réhospitalisations pour récidive. Pour comparer ce nouveau traitement aux corticoïdes inhalés, un groupe contrôle externe est constitué à partir d’une base de données administrative comprenant les dispensations. Sont inclus dans ce groupe contrôle externe des patients qui ont une dispensation de corticoïdes inhalés à la suite d’une hospitalisation pour BPCO. Ce design entrainera certainement un biais de sélection, car les patients pourront mettre quelques jours après leur sortie de l’hôpital pour aller chercher leur traitement à la pharmacie. Durant ce délai certains d’entre eux pourront être réhospitalisés pour des rechutes très précoces et ne seront pas inclus dans le groupe contrôle, car n’ayant pas eu de dispensations de corticoïdes inhalés bien qu’ayant eu une telle prescription sur leur ordonnance de sortie. Par contre, dans la monobras, les mêmes patients rechutant rapidement seront des comptabilités dans le groupe traité.
Parfois ces deux critères (vérifier l’éligibilité et être assigné à un traitement) se vérifient à plusieurs moments (même si dans le cas des groupes contrôles externes d’une étude expérimentale cette situation est moins fréquente qu’avec les études observationnelles classiques en raison de la définition d’un estimand plus strict).
Dans une étude monobras en oncologie, les patients étaient éligibles quelle que soit la ligne de leur traitement. Dans cette étude se côtoient donc des patients de première ligne (L1), de deuxième ligne (L2) ou plus (L2+). Une comparaison externe versus traitement standard est réalisée. Dans la source de données utilisée pour constituer ce groupe contrôle externe certains patients sont suivis depuis leur prise en charge initiale en L1 et l’historique de leur ligne successive est aussi enregistré. Ces patients vont présenter à plusieurs reprises le doublet : vérification des critères d’éligibilité et débuter un traitement (lors de leur L1 puis lors de leur passage en L2, L3, etc.). En d’autres termes ils pourraient servir de contrôle plusieurs fois : pour un patient inclus dans la monobras en L1, pour un patient inclus en L2, etc.
Différentes options sont possibles pour ces situations : tirage au sort parmi ces multiples possibilités, inclure plusieurs fois le même patient dans le groupe contrôle en tenant compte de cette réplication au niveau statistique, réalisation d’émulation séquentielle de plusieurs essais puis pooling de ces essais [198] [199] [185] , clonage de ces patients puis prise en compte de la réplication engendrée ou time-conditional PS.
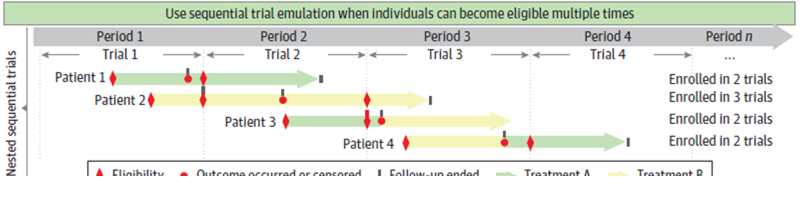
Figure 18 – principe de l’émulation séquentielle d’essais [200] .
Pour les groupes contrôles non traités , le suivi débutera à partir du moment où le patient vérifie les critères d’éligibilité et ne reçoit pas de traitement (avec une tolérance temporelle pour prendre en compte des délais en prescription et dispensation par exemple pour capter une prescription ou un début de traitement à cet instant alors que l’information apparaitra à une date légèrement différée du fait du temps de latence lié par exemple à la dispensation : temps pour le patient d’aller à la pharmacie pour récupérer son traitement par exemple).
Pour ces groupes contrôles non traités, il est indispensable que l’éligibilité soit déterminée à un instant donné sans tenir compte de ce qui se passera dans le futur de cet instant pour éviter le risque de biais de sélection (cf. section 17). Pour cela il est dangereux de ne retenir que des patients qui ne recevront jamais le traitement durant la période où il serait éligible. Si un patient reçoit le traitement au-delà de l’instant où il vérifie les critères d’éligibilité pour être dans un groupe non traité, cela ne doit pas entrainer son exclusion de ce groupe. En termes d’émulation cette situation correspondra à celle du recours à un traitement de secours dans un essai randomisé ou à un écart au protocole ou un retrait volontaire du patient de l’essai. Ainsi l’inclusion dans le groupe contrôle externe non traité d’un patient qui recevra après le t0 le traitement étudié est conforme à ce qui peut se passer dans le groupe contrôle d’un essai randomisé. Cela conduira donc à des mises sous traitement dans le groupe contrôle externe tout comme cela arrive dans un essai clinique où ces patients sont bien entendu maintenu dans l’analyse en intention de traité
Un essai monobras d’un nouveau traitement IV inclus des patients avec un cancer du poumon non à petites cellules nouvellement diagnostiqués (non traité auparavant). Les patients sont inclus dans l’étude monobras (t0) quant à une consultation (visite 0) le diagnostic de certitude peut être porté sur la base de l’imagerie et de l’histologie et que les autres critères d’éligibilité sont remplis. Et le traitement est débuté dès qu’un rendez-vous en hôpital de jour est obtenu (ne devant pas excéder 1mois d’attente).
Le groupe contrôle de patients traités par l’immunochimiothérapie standard de ce cancer issu d’un registre de la pathologie.
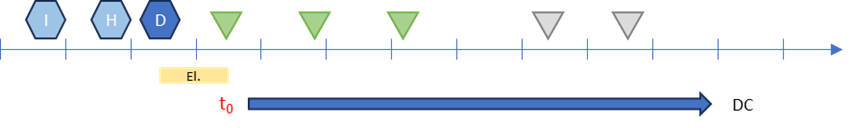
Dans la vraie vie, le diagnostic (D) est porté lors d’une consultation lorsque les résultats de l’imagerie (I) et de l’histologie (H) sont disponibles. Le traitement est décidé (prescription P) rapidement après lors d’une réunion de concertation pluridisciplinaire et le premier cycle administré quelques jours après.
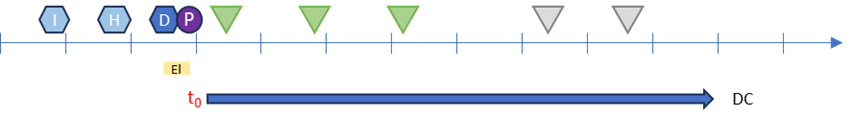
Le t0 correspondra à la date de cette réunion de concertation (P) qui coïncide avec le fait que le patient est devenu éligible (El.) depuis la disponibilité de l’imagerie et de l’histoogie, et qu’il est assigné au traitement contrôle (prescription/réunion de concertation). Il se peut d’ailleurs que le diagnostic soit établi que lors de cette réunion et donc établissement de l’éligibilité et assignation au traitement coïncide.
Le suivi se poursuivra jusqu’au décès du patient ou à la date de point que le traitement soit poursuivi, interrompue, changer ou que le patient progresse et passe en deuxième ligne (analyse en intention de traiter, correspondant à un estimand du type : « effet d’être assigné en première ligne à un traitement de type immunochimiothérapie ».
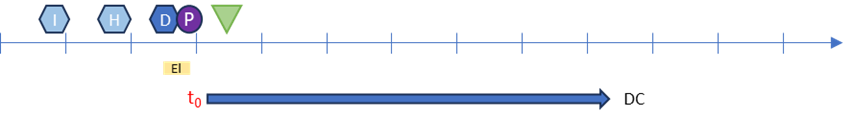
Si la notion de prescription ne transparait pas dans la source de données, le t0 sera la date de l’administration du premier cycle du traitement.
[22] La notion de prescription correspond à celle d’être assigné à un traitement par la randomisation.