2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
§ Cas particulier du groupe contrôle non traité
§ Captation des patients perdus de vue
18.2 Représentation graphique du processus d’extraction des données de l’étude
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
Certaines comparaisons externes impliquent un groupe contrôle non traité si aucun traitement n’est disponible pour l’indication visée par le nouveau traitement. C’est par exemple le cas dans les maladies rares lorsque la comparaison se veut versus l’histoire naturelle de la maladie.
Dans le cas du traitement d’un événement aigu, la date de ce dernier servira de t0. Mais pour les maladies chroniques, où le traitement étudié est débuté durant la maladie, indépendamment d’un événement aigu, se pose alors la question de déterminer la date de début du non-traitement.
Dans cette situation, l’éligibilité est vérifiée à de nombreux temps sans qu’il soit possible d’en privilégier un. De nombreuses options sont possibles [201] [189] [188] [192] [191] [197] .
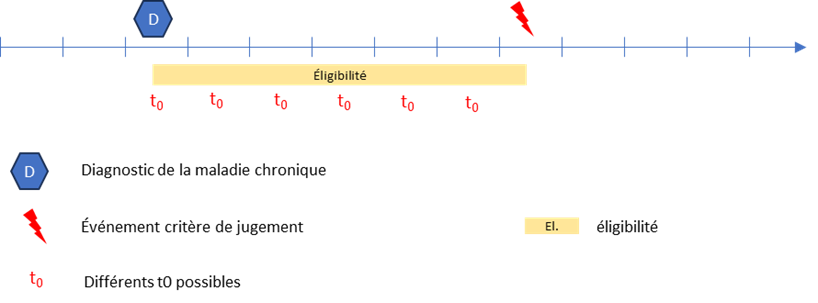
Une approche consiste à émuler une série séquentielle d’essais, par exemple tous les mois de la fenêtre temporelle considérée, ce qui permet de prendre en compte tous les temps durant lesquels un patient est éligible [202] [203] . Ensuite tous les essais émulés générés sont poolés ensemble pour donner le résultat de l’étude. Un même patient est pourra donc participer à plusieurs essais émulés avec plusieurs t0. Cette redondance des patients doit être prise en compte dans l’analyse statistique. L’avantage de cette méthode, qui semble s’imposer par rapport aux autres, est d’éviter de choisir un t0 parmi plusieurs possibles.