4 L’évaluation des marqueurs prédictifs
4.1 Etudes « treament only » , valeur pronostique sous traitement
4.1.1 Principe des études « treatment only »
4.1.2 Sensibilité au biais de publication
4.2 Études évaluant la valeur prédictive d’un marqueur
4.2.1 Analyses en sous-groupes exploratoires
4.2.1.1 Limites méthodologiques de l’approche exploratoire
4.2.1.2 Retour sur les limites des analyses « treatment only »
4.2.1.3 Limites de la recherche post hoc de marqueurs prédictifs
4.2.2 Analyses en sous-groupes de confirmation
4.2.3 Le design d’interaction biomarqueur-traitement
4.2.3.3 Inconvénients, limites
5 La personnalisation sur le risque de base
7 L’évaluation de l’utilité clinique par les essais de stratégie
La recherche de manière anticipée et prospective de la valeur prédictive d’un marqueur au sein même de l’essai pivot du traitement permet de solutionner toutes les problématiques méthodologiques rencontrées dans la validation à postériori (cf. section 4.2.1). Tous les principes méthodologiques de la recherche de preuves formelles peuvent être ainsi mis en œuvre : respect de la démarche hypothético-déductive avec une formulation à priori de l’hypothèse que le marqueur est prédictif, le sens de l’interaction sera aussi préspécifié par hypothèse ; intégration de la recherche de l’interaction marqueur-traitement dans le plan de contrôle du risque alpha global ; calcul de la puissance nécessaire pour conclure sur cette interaction ; etc.
Ces essais ont ainsi pour objectif de démontrer en premier le bénéfice clinique du traitement, mais aussi d’évaluer un marqueur prédictif candidat. Pour cela, ces essais, incluent des patients aussi bien marqueur positif que marqueur négatif. Très souvent la randomisation est stratifiée sur ce marqueur (et dans ce cas ce type d’étude est proche du design d’interaction, cf. section 4.2.3).
La recherche du bénéfice du traitement va être effectuée chez les patients marqueurs positifs (qui sont en théorie ceux le plus susceptible d’avoir un bénéfice du traitement si celui s’avère efficace) et aussi chez les patients marqueurs négatifs (ou chez tous les patients, quelle que soit la valeur du marqueur). Cette multiplicité de comparaison est alors prise en compte dans le plan de contrôle du risque alpha global de façon tout à fait conventionnelle soit par hiérarchisation soit par répartition du risque alpha.
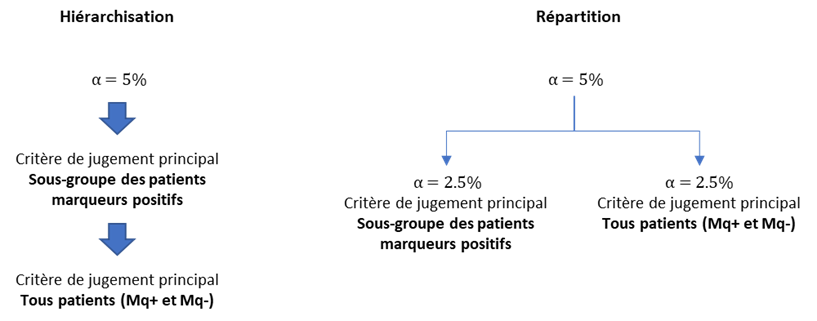
De plus en plus, un plan complexe de contrôle du risque alpha est employé mêlant hiérarchisation, répartition et recyclage du risque alpha (cf. exemple IMvigor 110 ci-dessous).
Exemple de répartition du risque alpha
L’erlotinib a été évalué versus placebo comme traitement de maintenance après chimiothérapie dans le cancer du poumon par l’essai SATURN [66] . Le critère de jugement principal était la PFS. À priori il était envisagé que le niveau d’expression de l’EGFR pouvait être un marqueur prédictif du bénéfice de l’erlotinib (avec un bénéfice uniquement en cas de surexpression de cette protéine mesurée par immunohistochimie). Cependant il était aussi possible que le traitement apporte un bénéfice indépendamment de ce marqueur et l’essai a inclus les patients positifs et négatifs.
“We designed the phase 3, placebo-controlled Sequential Tarceva in Unresectable NSCLC (SATURN; BO18192) study to investigate the effect of erlotinib as maintenance therapy on PFS in patients with non-progressive disease following first-line platinum-doublet chemotherapy. We assessed PFS in the overall population and in patients with tumours that over-express EGFR.”
La recherche de la valeur prédictive de ce marqueur a été intégrée dans le plan de contrôle du risque alpha global en répartissant le risque alpha global de 5% entre le sous-groupe EGFR positif (2%) et l’analyse globale de tous les patients (3%) :
The alpha level of 5% was split between the two coprimary endpoints: 3% for all patients and 2% for patients with EGFR immunohistochemistry-positive tumours.
Un bénéfice de l’erlotinib en termes de PFS est observé aussi bien dans le sous-groupe des patients EGFR positifs (HR 0·69, 0·58–0·82; p<0·0001) que chez tous les patients (HR 0·71, 95% CI 0·62–0·82; p<0·0001).
On peut remarquer que le test de l’efficacité de l’erlotinib chez les patients négatifs n’était pas prévu, car celui-ci ne correspond pas à une éventualité de démonstration spécifique de l’intérêt du traitement.
La logique de ces essais, bien illustrée par l’exemple précédent de l’erlotinib, est celle des essais pivots, c’est-à-dire produire des démonstrations de l’intérêt du traitement (d’arguments permettant d’obtenir une AMM ou une place dans la stratégie thérapeutique). Le marqueur prédictif pressenti est présent dans ces études pour gérer l’éventualité que le traitement n’ait une activité qu’en cas de présence de ce marqueur. Dans ce cas, l’étude le démontrera formellement ; contrairement à un essai qui n’aurait pas anticipé cette éventualité et où, les patients marqueurs positifs ne seraient qu’un sous-groupe ordinaire, incapable de fournir des démonstrations. Ainsi si l’essai est concluant sur l’ensemble des patients, la question du marqueur prédictif disparait (en partie, cf. infra). En revanche, si l’essai échoue à montrer un bénéfice sur l’ensemble des patients, mais donne un résultat statistiquement significatif chez les patients marqueurs positifs, il démontrera formellement le bénéfice du traitement chez ces patients. À ce moment la valeur prédictive du marqueur aura aussi été démontrée. Ces 2 résultats permettront de positionner le traitement et son marqueur prédictif dans la stratégie thérapeutique.
Cette approche a cependant une limite qui est celle de ne pas pouvoir conclure si le traitement des patients marqueurs négatif est justifié lorsque l’essai conclut à l’effet du traitement chez tous les patients [67] . Même si le traitement n’a aucun effet chez les marqueurs négatifs, le résultat global de l’essai peut être concluant, car il est principalement drivé par le bénéfice obtenu chez les patients marqueurs positifs. Il existe une dilution de l’effet chez les marqueurs positifs par l’absence d’effet chez les marqueurs négatifs, mais qui n’est pas suffisante pour conduire à un résultat global non concluant (par exemple si la proportion de marqueurs négatifs est faible ou si l’effet chez les marqueurs positifs est très important). Comme dans ces essais, le résultat spécifique obtenu chez les marqueurs négatifs n’est pas rapporté, il est difficile d’analyser ce point. Et même s’il est rapporté il va être difficile de conclure à l’exclusion de ces patients de la population cible, car on se retrouve devant un résultat de sous-groupe ordinaire, non nominalement significatif, avec toutes les limites de l’interprétation de ce type de résultat.
De plus en plus fréquemment, ces essais pivots couplant l’évaluation d’un nouveau traitement avec celui d’un ou plusieurs marqueurs prédictifs potentiels de son bénéfice utilisé des plans de contrôle du risque alpha global optimisés donc complexes.
L’essai IMpower 150 a évalué l’atezolizumab en première ligne du traitement du cancer du poumon non à petite cellule non épidermoïde métastatique [68] . Il était envisagé qu’un marqueur Teff-high pourrait être prédictif sur la base des résultats d’un essai précédent (OAK). La démonstration spécifique du bénéfice chez les marqueurs positifs (Teff-high) a été intégrée à un plan de contrôle du risque alpha global qui repose sur une répartition du risque alpha global entre les 2 critères de jugements PFS et OS. Pour la PFS, ce risque alpha attribué (0.012) est ensuite à nouveau réparti, de manière égale, entre la recherche de l’effet de l’atezolizumab sur la PFS uniquement chez les patients Teff-high WT (alpha 0.006) et la recherche de l’effet de l’atezolizumab chez tous les patients (ITT-WT). L’effet de l’atezolizumab est ensuite recherché chez tous les patients avec une réallocation du risque alpha en provenance de la PFS. Le risque alpha disponible pour l’OS dépend ainsi des résultats obtenus au niveau delà PFS.