4 L’évaluation des marqueurs prédictifs
4.1 Etudes « treament only » , valeur pronostique sous traitement
4.1.1 Principe des études « treatment only »
4.1.2 Sensibilité au biais de publication
4.2 Études évaluant la valeur prédictive d’un marqueur
4.2.1 Analyses en sous-groupes exploratoires
4.2.1.1 Limites méthodologiques de l’approche exploratoire
4.2.1.2 Retour sur les limites des analyses « treatment only »
4.2.1.3 Limites de la recherche post hoc de marqueurs prédictifs
4.2.2 Analyses en sous-groupes de confirmation
4.2.3 Le design d’interaction biomarqueur-traitement
4.2.3.1 Exemple - Essai PROSE
4.2.3.3 Inconvénients, limites
5 La personnalisation sur le risque de base
7 L’évaluation de l’utilité clinique par les essais de stratégie
Une signature protéomique a évalué comme candidat marqueur prédictif de la réponse à l’erlotinib dans le cancer du poumon non à petites cellules à l’aide d’un essai randomisé d’interaction dénommé PROSE [69] . La randomisation entre erlotinib ou chimiothérapie a été stratifiée sur le résultat de la signature protéomine. Le critère de jugement principal était la survie globale (OS, overall survival) et l’hypothèse principale de l’essai était bien la mise en évidence d’une interaction : « and the primary hypothesis was the existence of a significant interaction between the serum protein test classification and treatment.”.
Au total 184 patients pour lesquels le test prédisait une bonne réponse à l’erlotinib (groupe Good, que l’on peut appeler marqueur positif, le but recherché étant d’identifier les patients « répondeurs ») et 79 patients avec un test prédisant une mauvaise réponse (groupe Poor, marqueur négatif) ont été randomisés entre erlotinib et chimiothérapie.
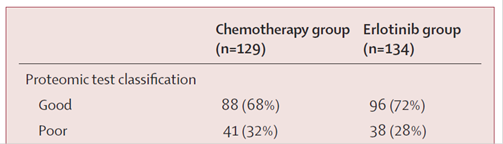
Les résultats obtenus sont les suivants :
OS |
PFS |
|
Mq+ : Good |
HR 1·06 [95% CI 0·77–1·46], p=0·714 |
HR 1·26 [95% CI 0·94–1·69], p=0·129 |
Mq- : Poor |
HR 1·72 [95% CI 1·08–2·74], p=0·022 |
HR 1·51 [95% CI 0·96–2·38], p=0·078 |
Interaction |
P interaction=0·017 |
P interaction=0·268 |
La figure suivante donne la représentation graphique de ces résultats :
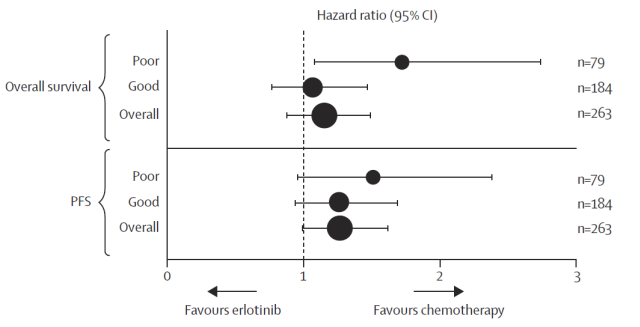
Une interaction statistiquement significative est trouvée pour l’OS (p=0.017). Pour les patients marqueurs négatifs (classification en Poor), l’erlotinib s’avère inférieur à la chimiothérapie. Ce résultat est compatible avec l’hypothèse. En effet, si le marqueur identifie correctement patients répondeurs et patients non répondeurs, les patients négatifs dans le groupe erlotinib se retrouvent comme s’ils n’étaient pas traités. Dans ce cas, l’erlotinib est attendu inférieur à la chimiothérapie (qui apporte un bénéfice indépendamment du statut sur le marqueur).
Cependant pour les patients marqueurs positifs (classification en Good), qui devraient être des patients qui répondent à l’erlotinib, le résultat est paradoxal en montrant une tendance à une infériorité de l’erlotnib par rapport à la chimiothérapie sur la PFS. Globalement, dans une analyse sans tenir compte de la signature protéomique, l’erlotinib ne montre dans cet essai aucun bénéfice en termes de PFS et d’OS.
Comme l’essai ne montre pas la supériorité de l’erlotinib chez les patients positifs et que l’interaction est l’inverse de celle qui était attendue, il est impossible de conclure à la valeur prédictive « pratique » de ce marqueur. Comme le résultat est inverse par rapport à l’hypothèse, il s’agirait d’une conclusion purement exploratoire sans intérêt pratique. Cet exemple illustre bien le fait que l’interaction ne fait pas tout dans la validation d’un marqueur prédictif (cf. section 2.1), encore faut-il qu’un bénéfice soit trouvé chez les patients marqueurs positifs et qu’il soit possible de conclure que les patients marqueurs négatifs ne tirent aucun bénéfice cliniquement pertinent du traitement (pour éviter de les priver à tort d’un traitement potentiellement utile pour eux)